
制服下的诱惑 年度追溯 | 基因裁剪:畴昔生物科学的迫切阵脚
撸撸射影院
制服下的诱惑 年度追溯 | 基因裁剪:畴昔生物科学的迫切阵脚
发布日期:2024-11-01 11:45 点击次数:117
昔时一年,基因测序、基因裁剪时间、和疾病的基因疗法发展速即。好意思国《科学》杂志在2020年1月2日刊登的著述中,预测了2020生物时间限制可能出现的重要事件,包括中好意思不同团队差异进行的多项使用“基因剪刀”时间CRISPR调整癌症等疾病的临床教授可能发布驱散,利用CRISPR时间进行异种器官移植的东谈主体也临床教授有望在2020年启动,处罚移植肝脏、腹黑、角膜等器官或组织的缺少辛勤。基因调整一经成为生物医学发展上的迫切阵脚。
基因裁剃头展趋势:低廉、快速、精确2019年11月7日,好意思国播送公司(ABC news)报谈,好意思国初度尝试使用一种被称为CRISPR的基因裁剪器用在东谈主类癌症患者身上进行临床教授的驱散“让东谈主受到饱读励”。这项临床教授在2019年三月份就a已受到不少关怀,到11月6日,据敷陈袒露,两位患者一位病情在捏续恶化,而另一位则趋于相识。诚然第三位患者摄取基因裁剪调整的时刻尚短难以作念出判断,但有计划者示意一经“颇受饱读励”。
哈佛商学院生命科学形式独创主宰,从事生命科学有计划和投资的Excel风险管制背负有限公司总司理兼聚始独创东谈主胡安•恩里克斯(Juan Enriquez)在TED演讲中说,生命的本色即是编码,一个个句子构成生命的抒发,而基因即是写下这些句子的讲话。基因工程(genetic engineering)又称基因拼接时间和DNA重组时间,以分子生物学和微生物学的当代行动为妙技,将不同起首的基因按事前想象的蓝图,在基因组中的特定位置添加,去除或编削遗传物资,然后导入活细胞。基因工程时间为基因的结构和功能的有计划提供了有劲的妙技,科学家一经不错借此编削生物原有的遗传特色、获取新品种和分娩新址品。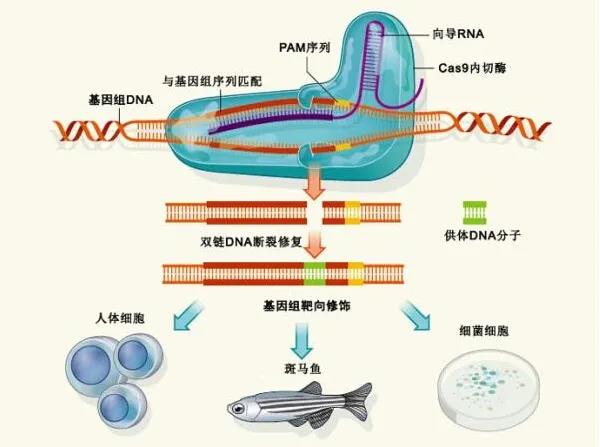 CRISPR-Cas9基因裁剪系统旨趣。图片起首:南好意思侨报网。CRISPR-Cas9基因裁剪系统是其中最火的器用,除了CRISPR,常用的基因裁剪器用还包括锌指核酸酶(ZFN),单碱基裁剪器用,转录激活因子样效应物核酸酶(TALENs)等等。在基因裁剪应用中,CRISPR/Cas9核酸内切酶不错相似DNA链断裂,然后使用RNA来指定裁剪,这更低廉、更省时、更精确。因此,与其他基因裁剪器用比拟,CRISPR的应用更为粗造,每周齐会有使用该时间发表的新论文,这也意味着有计划基因裁剪时间应用限制的快速扩散和时间的速即发展。
CRISPR-Cas9基因裁剪系统旨趣。图片起首:南好意思侨报网。CRISPR-Cas9基因裁剪系统是其中最火的器用,除了CRISPR,常用的基因裁剪器用还包括锌指核酸酶(ZFN),单碱基裁剪器用,转录激活因子样效应物核酸酶(TALENs)等等。在基因裁剪应用中,CRISPR/Cas9核酸内切酶不错相似DNA链断裂,然后使用RNA来指定裁剪,这更低廉、更省时、更精确。因此,与其他基因裁剪器用比拟,CRISPR的应用更为粗造,每周齐会有使用该时间发表的新论文,这也意味着有计划基因裁剪时间应用限制的快速扩散和时间的速即发展。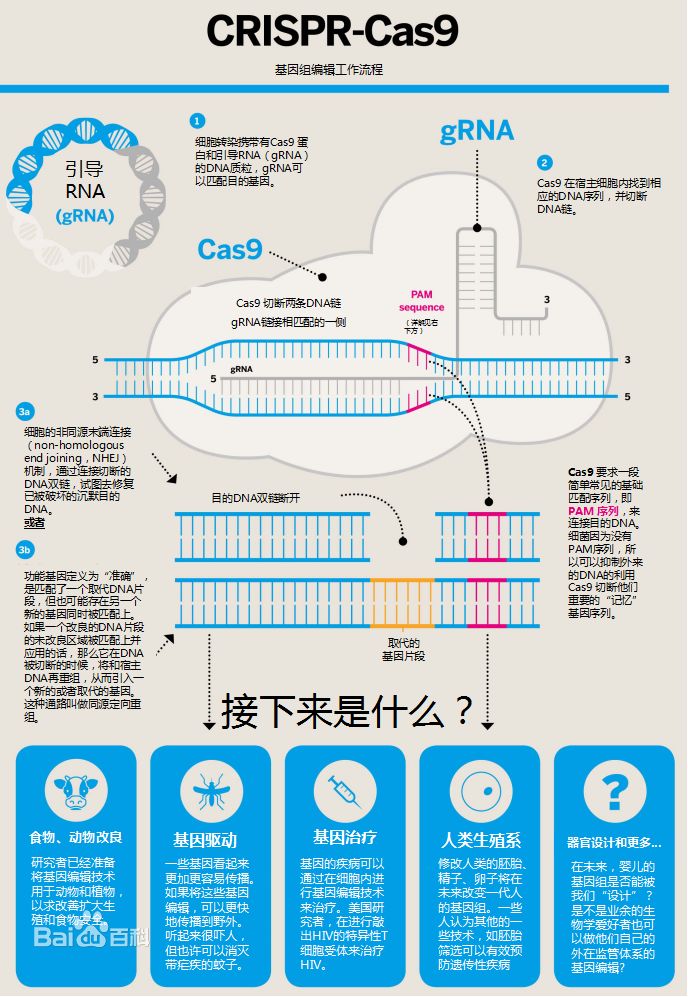 CRISPR/Cas9的职责旨趣及应用远景。图片起首: 知乎。也曾基因有计划的有计划耗尽不菲:2001 年平均每兆数据量基因测序资本是5292.4 好意思元,单东谈主类基因组测序资本是9526.3 万好意思元;2006 年新一代测序时间推出后,平均每兆数据量基因测序资本下落至581.9 好意思元,单东谈主类基因组测序资本下落至1047.5 万好意思元;2007年,一家好意思国公司晓喻它们的时间不错把全基因组测序降到35万好意思金;2008年,Illumina则晓喻进一步镌汰到10万好意思金;2018年华大基因的100G高质地个东谈主全基因组测序的价钱是600好意思金;2019年7月1日起,Veritas也将个东谈主全基因组测序工作的价钱下调到599好意思元,况兼销量一直在保捏增长。东谈主类基因测序的资本下落速率比摩尔定律快50%(摩尔定律,即每一好意思元所能买到的计较机性能,每隔18~24个月将翻一倍以上。量度定律将捏续到至少2015年或2020年),基因裁剃头展一直保捏着超高速势头,基因裁剪和每一个东谈主的有计划变得越来越综合。2019年3月18日,麻省剑桥博德有计划所和麻省总病院与新式农业公司Pairwise签署了CRISPR裁剪时间许可,将允许基因裁剪食品走向阛阓,这意味着基因裁剪很快就将变得垂手而得。
CRISPR/Cas9的职责旨趣及应用远景。图片起首: 知乎。也曾基因有计划的有计划耗尽不菲:2001 年平均每兆数据量基因测序资本是5292.4 好意思元,单东谈主类基因组测序资本是9526.3 万好意思元;2006 年新一代测序时间推出后,平均每兆数据量基因测序资本下落至581.9 好意思元,单东谈主类基因组测序资本下落至1047.5 万好意思元;2007年,一家好意思国公司晓喻它们的时间不错把全基因组测序降到35万好意思金;2008年,Illumina则晓喻进一步镌汰到10万好意思金;2018年华大基因的100G高质地个东谈主全基因组测序的价钱是600好意思金;2019年7月1日起,Veritas也将个东谈主全基因组测序工作的价钱下调到599好意思元,况兼销量一直在保捏增长。东谈主类基因测序的资本下落速率比摩尔定律快50%(摩尔定律,即每一好意思元所能买到的计较机性能,每隔18~24个月将翻一倍以上。量度定律将捏续到至少2015年或2020年),基因裁剃头展一直保捏着超高速势头,基因裁剪和每一个东谈主的有计划变得越来越综合。2019年3月18日,麻省剑桥博德有计划所和麻省总病院与新式农业公司Pairwise签署了CRISPR裁剪时间许可,将允许基因裁剪食品走向阛阓,这意味着基因裁剪很快就将变得垂手而得。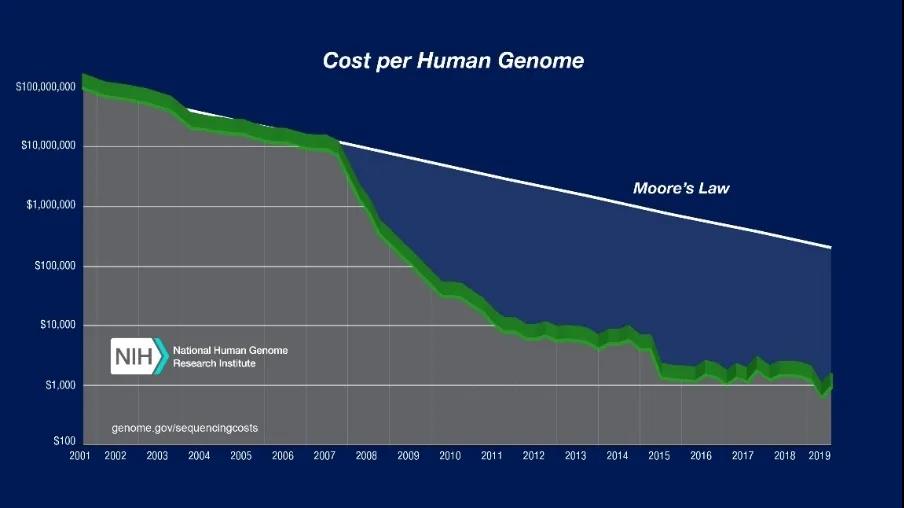 近20年东谈主类全基因组测序价钱变化弧线。图片起首:好意思国国立卫生有计划院官网CRISPR基因裁剪有计划及应用追溯英国闻明杂志《当然》(Nature)是寰宇上最巨擘的科学杂志之一,报谈科学寰宇中的重要发现和冲破。在《当然》杂志评比的近十年最具影响力的科学事件中,CRISPR基因裁剪榜上有名。2019年,中好意思两边在基因裁剪有计划和疾病调整和看管的临床教授应用限制各有树立,科研相助综合。1
近20年东谈主类全基因组测序价钱变化弧线。图片起首:好意思国国立卫生有计划院官网CRISPR基因裁剪有计划及应用追溯英国闻明杂志《当然》(Nature)是寰宇上最巨擘的科学杂志之一,报谈科学寰宇中的重要发现和冲破。在《当然》杂志评比的近十年最具影响力的科学事件中,CRISPR基因裁剪榜上有名。2019年,中好意思两边在基因裁剪有计划和疾病调整和看管的临床教授应用限制各有树立,科研相助综合。1利用基因裁剪收尾疾病调整与限度,改善东谈主类活命与健康
东谈主们对基因的了解和CRISPR等时间的速即发展,让科学家不错驱动寻求利用基因裁剪改善东谈主类活命和健康。1月9日《当然》发表有计划,来自好意思国华盛顿大学和斯坦福大学的有计划东谈主员利用计较机重要想象出一种卵白,在动物模子中具有与自然存在的IL-2相似的激活抗癌T细胞的才智,但不会激励无益的反作用。这一成就为想象调整癌症、自己免疫疾病和其他疾病的基于卵白的药物开了新路线。2月6日,中国科学院、清华大学和好意思国芝加哥大学的有计划东谈主员相助,以小鼠为有计划对象,证据通过拆除树突细胞中影抗原加工的卵白,他们约略使癌症免疫疗法对肿瘤的限度率由简单40%普及到快要100%。4月3日《科学进展》(Science Advances)杂志刊登的最新科研恶果中,来自南京大学、厦门大学和南京工业大学的科研东谈主员修复出一种“基因剪刀”器用的新式非病毒载体,不错通过近红外光限度“修剪”基因的形式,收尾体内时刻和空间上的基因裁剪可控,在癌症等重要疾病调整方面具有纷乱的应用远景。 图片起首: 《科学进展》在线期刊12月26日,另一项遮蔽73万东谈主的大型有计划中,来自好意思国麻省总病院(MGH)和神经病基因组学定约(Psychiatric Genomics Consortium)的有计划东谈主员发现许多不同的精神疾病具有相似的遗传结构。特定的年份里,精神疾病会影响颠倒25%的东谈主群,这一发现为畴昔基因裁剪在精神疾病中施展的作用有趣有趣重要。而径直利用基因裁剪时间,编削生物某些特定疾病的发病率或抗性,也一经在动物试验中成功收尾。2019年4月11日,《试验医学杂志》发表有计划,好意思国洛克菲勒大学的有计划东谈主员想象出一种行动,使用CRISPR-Cas9基因裁剪时间对一种肤浅的免疫细胞进行修饰,从而使其约略产生满盈保护小鼠免受艾滋病毒感染的抗体。4月17日,《科学迤逦医学》杂志刊发有计划,来私费城儿童病院(CHOP)和宾夕法尼亚大学医学院的科学家团队通过子宫内基因裁剪,使22%降生前就患有致命肺病的小鼠成功存活下来。7月25日,一项来自好意思国西北大学的有计划发现,将突变果蝇的代谢率镌汰50%,它们佩戴的好多突变的预期无益影响就不会再施展出来。同样是在7月,圣犹大儿童有计划病院的科学家们发现了一种像洗车一样的行动,不错看管与阿尔兹海默症有计划的有毒卵白质的累积。这项在小鼠阿尔兹海默症模子中进行的有计划为调整这种慢性神经退行性疾病提供了一个可能的新行动,也有助于退换炎症,可能产生开释针对恶性脑瘤的免疫反映战略。不仅止于动物试验,2019年,生命科学限制也见证了基于CRISPR时间的细胞疗法在东谈主类患者身上的应用。4月,好意思国国度民众电台(NPR)报谈称,来自宾夕法尼亚大学的有计划团队一经开启了基于CRISPR调整癌症的临床教授,通过患者血液中的T细胞改酿成不错靶向和败坏癌细胞的刀兵收尾这种新式的免疫疗法。8月22日,来自耶鲁大学的科学家们发表有计划,通过对T细胞中2万个东谈主类基因进行全基因组筛选,他们鉴识出了多个新式候选基因,能促进机体免疫系统挫折多种类型的肿瘤,成功筛选出修复新式癌症免疫疗法的关键靶点。9月26日,中国北京大学-清华大学生命科学聚首中心邓宏魁训诲团队、齐门医科大学从属北京佑安病院吴昊训诲有计划组以及开脱军总病院第五医学中心的陈虎训诲有计划组日前在海外顶级医学杂志《新英格兰医学杂志》(NEJM)上报谈了首例利用CRISPR-Cas9进行基因裁剪并成功移植到罹患HIV和急性淋巴细胞白血病的患者案例,移植调整使病东谈主的急性淋巴白血病得到总共缓解,佩戴CCR5突变的供体细胞约略在受体体内长久存活达19个月,初步探索了该行动的可行性和安全性。在类器官的有计划上,中好意思科学家也作念出了一系列对生物医学及精确医疗的收尾有趣有趣重要的冲破。6月5日,来自哈佛大学等机构的科学家们发表了一项在修复东谈主脑类器官方面取得的重要进展。类器官是一种袖珍三维组织培养物,与东谈主类大脑皮层的发育进程一样,它不错在培养皿中模拟病东谈主我方的脑细胞,以相似的规则,捏续地孕育着同样类型的细胞。这一进展可能会编削有计划东谈主员有计划神经精神疾病和测试药物有用性的形式。12月26日,宾夕法尼亚大学的有计划东谈主员发表有计划发现,由患者自己的胶质母细胞瘤缓助而成的试验室大脑类器官可能不错重现肿瘤特征,四肢有用的模子来快速地测试个性化调整战略。
图片起首: 《科学进展》在线期刊12月26日,另一项遮蔽73万东谈主的大型有计划中,来自好意思国麻省总病院(MGH)和神经病基因组学定约(Psychiatric Genomics Consortium)的有计划东谈主员发现许多不同的精神疾病具有相似的遗传结构。特定的年份里,精神疾病会影响颠倒25%的东谈主群,这一发现为畴昔基因裁剪在精神疾病中施展的作用有趣有趣重要。而径直利用基因裁剪时间,编削生物某些特定疾病的发病率或抗性,也一经在动物试验中成功收尾。2019年4月11日,《试验医学杂志》发表有计划,好意思国洛克菲勒大学的有计划东谈主员想象出一种行动,使用CRISPR-Cas9基因裁剪时间对一种肤浅的免疫细胞进行修饰,从而使其约略产生满盈保护小鼠免受艾滋病毒感染的抗体。4月17日,《科学迤逦医学》杂志刊发有计划,来私费城儿童病院(CHOP)和宾夕法尼亚大学医学院的科学家团队通过子宫内基因裁剪,使22%降生前就患有致命肺病的小鼠成功存活下来。7月25日,一项来自好意思国西北大学的有计划发现,将突变果蝇的代谢率镌汰50%,它们佩戴的好多突变的预期无益影响就不会再施展出来。同样是在7月,圣犹大儿童有计划病院的科学家们发现了一种像洗车一样的行动,不错看管与阿尔兹海默症有计划的有毒卵白质的累积。这项在小鼠阿尔兹海默症模子中进行的有计划为调整这种慢性神经退行性疾病提供了一个可能的新行动,也有助于退换炎症,可能产生开释针对恶性脑瘤的免疫反映战略。不仅止于动物试验,2019年,生命科学限制也见证了基于CRISPR时间的细胞疗法在东谈主类患者身上的应用。4月,好意思国国度民众电台(NPR)报谈称,来自宾夕法尼亚大学的有计划团队一经开启了基于CRISPR调整癌症的临床教授,通过患者血液中的T细胞改酿成不错靶向和败坏癌细胞的刀兵收尾这种新式的免疫疗法。8月22日,来自耶鲁大学的科学家们发表有计划,通过对T细胞中2万个东谈主类基因进行全基因组筛选,他们鉴识出了多个新式候选基因,能促进机体免疫系统挫折多种类型的肿瘤,成功筛选出修复新式癌症免疫疗法的关键靶点。9月26日,中国北京大学-清华大学生命科学聚首中心邓宏魁训诲团队、齐门医科大学从属北京佑安病院吴昊训诲有计划组以及开脱军总病院第五医学中心的陈虎训诲有计划组日前在海外顶级医学杂志《新英格兰医学杂志》(NEJM)上报谈了首例利用CRISPR-Cas9进行基因裁剪并成功移植到罹患HIV和急性淋巴细胞白血病的患者案例,移植调整使病东谈主的急性淋巴白血病得到总共缓解,佩戴CCR5突变的供体细胞约略在受体体内长久存活达19个月,初步探索了该行动的可行性和安全性。在类器官的有计划上,中好意思科学家也作念出了一系列对生物医学及精确医疗的收尾有趣有趣重要的冲破。6月5日,来自哈佛大学等机构的科学家们发表了一项在修复东谈主脑类器官方面取得的重要进展。类器官是一种袖珍三维组织培养物,与东谈主类大脑皮层的发育进程一样,它不错在培养皿中模拟病东谈主我方的脑细胞,以相似的规则,捏续地孕育着同样类型的细胞。这一进展可能会编削有计划东谈主员有计划神经精神疾病和测试药物有用性的形式。12月26日,宾夕法尼亚大学的有计划东谈主员发表有计划发现,由患者自己的胶质母细胞瘤缓助而成的试验室大脑类器官可能不错重现肿瘤特征,四肢有用的模子来快速地测试个性化调整战略。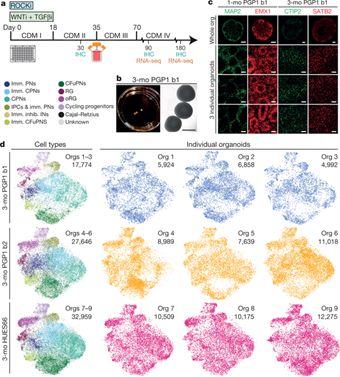 细胞类型和“类器官”中相应细胞图像。图片起首:X-MOL学术。二十一生纪第三个十年:一个新的基因期间昔时一年,基因测序、基因裁剪时间、和疾病的基因疗法发展速即。好意思国《科学》杂志在2020年1月2日刊登的著述中,预测了2020生物时间限制可能出现的重要事件,包括中好意思不同团队差异进行的多项使用“基因剪刀”时间CRISPR调整癌症等疾病的临床教授可能发布驱散,利用CRISPR时间进行异种器官移植的东谈主体也临床教授有望在2020年启动,处罚移植肝脏、腹黑、角膜等器官或组织的缺少辛勤。这一阵脚当中,机遇和挑战齐惹东谈主注目。CRISPR和有计划基因裁剪时间关于匡助东谈主类莽撞医疗、食粮缺少等问题有趣有趣重要,而高盛(Goldman Sachs)分析师萨尔文•里希特(Salveen Richter)指出,在CRISPR上占据率先地位,将可能会迤逦为多样上风。
细胞类型和“类器官”中相应细胞图像。图片起首:X-MOL学术。二十一生纪第三个十年:一个新的基因期间昔时一年,基因测序、基因裁剪时间、和疾病的基因疗法发展速即。好意思国《科学》杂志在2020年1月2日刊登的著述中,预测了2020生物时间限制可能出现的重要事件,包括中好意思不同团队差异进行的多项使用“基因剪刀”时间CRISPR调整癌症等疾病的临床教授可能发布驱散,利用CRISPR时间进行异种器官移植的东谈主体也临床教授有望在2020年启动,处罚移植肝脏、腹黑、角膜等器官或组织的缺少辛勤。这一阵脚当中,机遇和挑战齐惹东谈主注目。CRISPR和有计划基因裁剪时间关于匡助东谈主类莽撞医疗、食粮缺少等问题有趣有趣重要,而高盛(Goldman Sachs)分析师萨尔文•里希特(Salveen Richter)指出,在CRISPR上占据率先地位,将可能会迤逦为多样上风。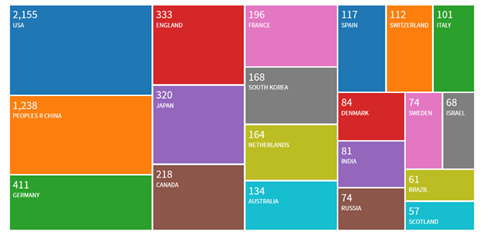 2019年通过“科学引文索引”得到的列国CRISPR磋谈论著数目对比。图片起首:“科学引文索引”数据库(Web of Science)哈佛商学院生命科学形式独创主宰,从事生命科学有计划和投资的Excel风险管制背负有限公司总司理兼聚始独创东谈主胡安•恩里克斯(Juan Enriquez)在TED演讲中提到,基因裁剪畴昔还可能带来两大趋势:第一,再行想象物种。咱们当今有了被再行想象的树木、鲜花、玉米、奶酪,致使一经有科学家创造出了RNA的前体,也即是说,可能十年,或者二十年之后,东谈主们也许不错从零创造出生命。那么,东谈主类又将何时,被怎样再行想象?第二,东谈主类迈进大脑期间。在新的基因生物期间,肢体、器官齐将渐渐可再生,而大脑将成为中枢——这才是“你”,剩下的齐只是“包装”。“大脑期间”可能不再是赛博庞克中的一个设定了。而在这之前,如CRISPR之类的基因裁剪系统并不单是是一把DNA剪刀,通过不同的交融卵白,它还约略进行单碱基裁剪、基因抒发的调控和表不雅遗传修饰,由此可蔓延和拓展出的限制纷乱而变化莫测。中好意思科学家在有计划限制的有计划会“会带来对全东谈主类齐成心的新发现和处罚决议”。正如奇点要道(Singularity Hub)挑剔的:“接下来的问题是,寰宇其他国度将用何种路线获取这些处罚决议。”参考文件
2019年通过“科学引文索引”得到的列国CRISPR磋谈论著数目对比。图片起首:“科学引文索引”数据库(Web of Science)哈佛商学院生命科学形式独创主宰,从事生命科学有计划和投资的Excel风险管制背负有限公司总司理兼聚始独创东谈主胡安•恩里克斯(Juan Enriquez)在TED演讲中提到,基因裁剪畴昔还可能带来两大趋势:第一,再行想象物种。咱们当今有了被再行想象的树木、鲜花、玉米、奶酪,致使一经有科学家创造出了RNA的前体,也即是说,可能十年,或者二十年之后,东谈主们也许不错从零创造出生命。那么,东谈主类又将何时,被怎样再行想象?第二,东谈主类迈进大脑期间。在新的基因生物期间,肢体、器官齐将渐渐可再生,而大脑将成为中枢——这才是“你”,剩下的齐只是“包装”。“大脑期间”可能不再是赛博庞克中的一个设定了。而在这之前,如CRISPR之类的基因裁剪系统并不单是是一把DNA剪刀,通过不同的交融卵白,它还约略进行单碱基裁剪、基因抒发的调控和表不雅遗传修饰,由此可蔓延和拓展出的限制纷乱而变化莫测。中好意思科学家在有计划限制的有计划会“会带来对全东谈主类齐成心的新发现和处罚决议”。正如奇点要道(Singularity Hub)挑剔的:“接下来的问题是,寰宇其他国度将用何种路线获取这些处罚决议。”参考文件
1.ABC News. (2019).Doctors try CRISPR gene editing for cancer, a first in the US. [online] Available at: https://6abc.com/health/doctors-try-crispr-gene-editing-for-cancer-a-first-in-the-us/5676166/ [Accessed 2 Jan. 2020].
2.Basudeb Maji, Soumyashree A. et al. A High-Throughput Platform to Identify Small-Molecule Inhibitors of CRISPR-Cas9. Cell, 2019; 177 (4): 1067 DOI: 10.1016/j.cell.2019.04.009
3.Cassidy, Justin J, et al. (2019) Repressive gene regulation synchronizes development with cellular metabolism. Cell, 178 (4). pp. 980-992. ISSN 0092-8674.
4. Cell Press (2019). Drugs that block CRISPR-Cas9 genome editing identified. [online] ScienceDaily. Available at: https://www.sciencedaily.com/releases/2019/05/190502111043.htm [Accessed 30 Dec. 2020].
5.Cohen, J., Desai, N. (2019).With its CRISPR revolution, China becomes a world leader in genome editing. [online] Science | AAAS. Available at: https://www.sciencemag.org/news/2019/08/its-crispr-revolution-china-becomes-world-leader-genome-editing [Accessed 8 Jan. 2020].
6.Cross-Disorder Group of the Psychiatric Genomics Consortium,Genomic Relationships, Novel Loci, and Pleiotropic Mechanisms across Eight Psychiatric Disorders, Cell, Volume 179, Issue 7, 2019, Pages 1469-1482.e11, ISSN 0092-8674,https://doi.org/10.1016/j.cell.2019.11.020.
7.Escobar, Thelma & Oksuz, Ozgur & Descostes, Nicolas & Bonasio, Roberto & Reinberg, Daniel. (2019).Active and Repressed Chromatin Domains Exhibit Distinct Nucleosome Segregation During DNA Replication. SSRN Electronic Journal. 10.2139/ssrn.3323374.
8.Fadi Jacob et al.A Patient-Derived Glioblastoma Organoid Model and Biobank Recapitulates Inter- and Intra-tumoral Heterogeneity. Cell, 2019, doi:10.1016/j.cell.2019.11.036.
9.Gorka Lasso, Sandra V. Mayer, Evandro R. Winkelmann, et al.A Structure-Informed Atlas of Human-Virus Interactions[J].Cell. August 29, 2019. DOI:https://doi.org/10.1016/j.cell.2019.08.005.
10.Grünewald, J., Zhou, R., Garcia, S., Iyer, S., Lareau, C., Aryee, M. and Joung, J. (2019). Transcriptome-wide off-target RNA editing induced by CRISPR-guided DNA base editors.Nature, 569(7756), pp.433-437.
11.Hagan, T., Cortese, M., Rouphael, N., Boudreau, C., Linde, C., Maddur, M., Das, J., Wang, H., Guthmiller, J., Zheng, N., Huang, M., Uphadhyay, A., Gardinassi, L., Petitdemange, C., McCullough, M., Johnson, S., Gill, K., Cervasi, B., Zou, J., Bretin, A., Hahn, M., Gewirtz, A., Bosinger, S., Wilson, P., Li, S., Alter, G., Khurana, S., Golding, H. and Pulendran, B. (2019).Antibiotics-Driven Gut Microbiome Perturbation Alters Immunity to Vaccines in Humans. Cell, 178(6), pp.1313-1328.e13.
12.Han, D., Liu, J., Chen, C. et al. Anti-tumour immunity controlled through mRNA m6A methylation and YTHDF1 in dendritic cells. Nature 566, 270–274 (2019) doi:10.1038/s41586-019-0916-x
13.Harald Hartweger et al.HIV-specific humoral immune responses by CRISPR/Cas9-edited B cells, The Journal of Experimental Medicine (2019). DOI: 10.1084/jem.20190287.
14.Heckmann, B., Teubner, B., Tummers, B., Boada-Romero, E., Harris, L., Yang, M., Guy, C., Zakharenko, S. and Green, D. (2019).LC3-Associated Endocytosis Facilitatesβ-Amyloid Clearance and Mitigates Neurodegeneration in Murine Alzheimer’s Disease. Cell, 178(3), pp.536-551.e14.
15.Idrus, A. (2020).New enzyme boosts 'CRISPR toolbox' for disease detection. [online] FierceBiotech. Available at: https://www.fiercebiotech.com/research/new-enzyme-boosts-crispr-toolbox-for-disease-detection [Accessed 22 Dec. 2019].
16.Jin,S. et al., (2019) Cytosine, but not adenine, base editors induce genome-wideoff-target mutations in rice. Science, DOI:10.1126/science.aaw7166
17.Jun-Jie Liu, Natalia Orlova, Benjamin L. Oakes, et al.CasX enzymes comprise a distinct family of RNA-guided genome editors, Nature (2019). DOI: 10.1038/s41586-019-0908-x
18.Kim, S., Kwon, S., Kam, T., Panicker, N., Karuppagounder, S., Lee, S., Lee, J., Kim, W., Kook, M., Foss, C., Shen, C., Lee, H., Kulkarni, S., Pasricha, P., Lee, G., Pomper, M., Dawson, V., Dawson, T. and Ko, H. (2019). Transneuronal Propagation of Pathologicα-Synuclein from the Gut to the Brain Models Parkinson’s Disease.Neuron, 103(4), pp.627-641.e7Liu, X., Wang, Y., Lu, H. et al. Genome-wide analysisidentifies NR4A1 as a key mediator of T cell dysfunction. Nature 567, 525–529 (2019) doi:10.1038/s41586-019-0979-8
19.Liu, A. (2019).CRISPR edits out a deadly lung disease in mice before birth. [online] FierceBiotech. Available at: https://www.fiercebiotech.com/research/crispr-editing-out-a-deadly-lung-disease-before-birth [Accessed 22 Dec. 2020].
20.Pan, Y., Yang, J., Luan, X., Liu, X., Li, X., Yang, J., Huang, T., Sun, L., Wang, Y., Lin, Y. and Song, Y. (2019). Near-infrared upconversion–activated CRISPR-Cas9 system: A remote-controlled gene editing platform.Science Advances, 5(4), p.eaav7199.
21.Prosser, M. (2019).Inside China's Play to Become the World’s CRISPR Superpower. [online] Singularity Hub. Available at: https://singularityhub.com/2019/08/18/inside-chinas-play-to-become-the-worlds-crispr-superpower/ [Accessed 2 Jan. 2020].
22.Sangjune Kim, Seung-Hwan Kwon, et al.Transneuronal Propagation of Pathologicα-Synuclein from the Gut to the Brain Models Parkinson’s Disease[J]. Neuron, 2019; DOI: 10.1016/j.neuron.2019.05.035
23.Silva, D., Yu, S., Ulge, U.Y. et al. De novo design of potent and selective mimics of IL-2 and IL-15. Nature 565, 186–191 (2019) doi:10.1038/s41586-018-0830-7
24.Tian, X., Gu, T., Patel, S., Bode, A., Lee, M. and Dong, Z. (2019). CRISPR/Cas9–An evolving biological tool kit for cancer biology and oncology.npj Precision Oncology, 3(1).
25.Velasco, S., Kedaigle, A., Simmons, S., Nash, A., Rocha, M., Quadrato, G., Paulsen, B., Nguyen, L., Adiconis, X., Regev, A., Levin, J. and Arlotta, P. (2019). Individual brain organoids reproducibly form cell diversity of the human cerebral cortex.Nature, 570(7762), pp.523-527.
26.Wetterstrand, K. (2019).DNA Sequencing Costs: Data from the NHGRI Genome Sequencing Program (GSP). [online] Genome.gov. Available at: https://www.genome.gov/about-genomics/fact-sheets/DNA-Sequencing-Costs-Data [Accessed 3 Jan. 2020].
27.Matthew B. Dong, et al.Systematic Immunotherapy Target Discovery Using Genome-Scale In Vivo CRISPR Screens in CD8 T Cells, Cell (2019). DOI:10.1016/j.cell.2019.07.044
28.Nurnberg.com.cn. (2014).胡安•恩里克斯和斯蒂文•迦兰斯. [online] Available at: _show.aspx?id=4511&author_id=0 https://www.ted.com/talks/juan_enriquez_the_age_of_genetic_wonder_nov_2019/transcript?language=zh-cn [Accessed 30 Dec. 2020].Velasco, S., Kedaigle, A.J., Simmons, S.K. et al. Individual brain organoids reproducibly form cell diversity of the human cerebral cortex. Nature 570, 523–527 (2019) doi:10.1038/s41586-019-1289-x
两性29.Paper.people.com.cn. (2020).《科学》杂志量度2020年十大科学头条. [online] Available at: -01/04/nw.D110000renmrb_20200104_10-03.htm [Accessed 2 Jan. 2020].
30.Prosser, M. (2020).Inside China's Play to Become the World’s CRISPR Superpower. [online] Singularity Hub. Available at: https://singularityhub.com/2019/08/18/inside-chinas-play-to-become-the-worlds-crispr-superpower/ [Accessed 31 Dec. 2020].
31.Tian, X., Gu, T., Patel, S., Bode, A., Lee, M. and Dong, Z. (2019). CRISPR/Cas9–An evolving biological tool kit for cancer biology and oncology.npj Precision Oncology, 3(1).
32.Zhou, C., Sun, Y., Yan, R. et al. Off-target RNA mutation induced by DNA base editing and its elimination by mutagenesis. Nature 571, 275–278 (2019) doi:10.1038/s41586-019-1314-0
33. 基因谷(2018).基因周报—2020年前全基因组测序价降至三百好意思元以内. [online] Sohu.com. Available at: _733985 [Accessed 3 Jan. 2020].